Única News
Da Redação
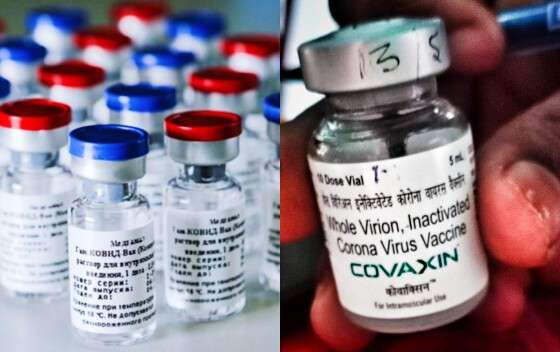
O gerente-geral da Agência Nacional de Vigilância Sanitária (Anvisa), Gustavo Mendes, explicou de que forma as vacinas Sputnik V, da Rússia, e Covaxin, da Índia, serão aplicadas no Brasil, após a agência aprovar, de forma controlada e com restrições, a utilização dos imunizantes no país.
A diretoria colegiada da Anvisa autorizou por 4 votos a 1, nesta sexta-feira (04), a importação temporária e excepcional das vacinas, mas com restrições para o uso de ambas.
Segundo Gustavo Mendes, os dados apresentados pelas farmacêuticas russa e indiana ainda não respondem a todos os questionamentos da Anvisa; entretanto, a agência adotou uma estratégia para que possa ser feito o uso controlado dos imunizantes.
"Nosso parecer foi baseado nos dados que a gente recebeu até o momento, que são dados limitados que não demonstram eficácia, segurança e qualidade desses produtos; e os relatórios que foram apresentados, no caso da Sputnik e da Covaxin, não respondem a todas as nossas perguntas", disse.
À CNN, Gustavo Mendes exemplificou como uma das principais condicionantes funcionará, no caso da vacina Sputnik V, da Rússia, e um de seus componentes.
"Condicionantes que a gente entende que minimizam os riscos. Por exemplo, na questão do adenovírus replicante, na Sputnik, muito discutida; a nossa determinação foi que o INCQS, um laboratório brasileiro, pudesse fazer a análise dessas vacinas que virão ao Brasil e garantir que não tenha esse adenovírus replicante, essa é uma condicionante que exemplifica tudo que foi pensado para minimizar esse risco nas pessoas", afirmou.
"Essa vacina não deverá ser utilizada por pessoas com hipersensibilidade a qualquer um dos componentes da fórmula, grávidas, lactantes, menores de 18, mulheres em idade fértil que querem engravidar, enfermidades graves ou não controladas e antecedentes de anafilaxia", disse Gustavo.
Pessoas que tenham recebido outra vacina contra covid-19, febre, HIV, hepatite B ou C, que tenham se vacinado nas 4 semanas anteriores, tenham recebido imunoglobulinas ou hemoderivados 3 meses antes, tenham recebido tratamentos com imunossupressores, citotóxicos, quimioterapia ou radiação 36 meses, tenham recebido terapias com biológicos incluindo anticorpos anticitocinas e outros anticorpos.
Ao todo 17 estados compraram 66 milhões de doses. Mato Grosso adquiriu 1,2 milhão. O processo analisado pela Anvisa, porém, são referentes aos estados da Bahia, Maranhão, Sergipe, Ceará, Pernambuco, Piauí - a aprovação representa um significativo avanço no processo de aquisição para MT.
ENTRE EM NOSSO CANAL AQUI
RECEBA DIARIAMENTE NOSSAS NOTÍCIAS NO WHATSAPP! GRUPO 1 - GRUPO 2 - GRUPO 3